Artigos Originais
Flora, estrutura diamétrica, hipsométrica e grupos ecológicos de um fragmento de Cerrado do Cariri, Tocantins
Flora, diametric and hypsometric structures, and ecological groups in a Cerrado fragment of Cariri, Tocantins
Flora, estructura diamétrica, hipsométrica y grupos ecológicos de un fragmento de Cerrado del Cariri, Tocantins
Flora, estrutura diamétrica, hipsométrica e grupos ecológicos de um fragmento de Cerrado do Cariri, Tocantins
Vértices (Campos dos Goitacazes), vol. 20, núm. 1, 2018
Instituto Federal de Educação, Ciência e Tecnologia Fluminense

Esta obra está bajo una Licencia Creative Commons Atribución 4.0 Internacional.
Recepción: 19 Diciembre 2016
Aprobación: 08 Febrero 2018
Resumo: O objetivo foi identificar a composição florística, destacar as espécies raras e/ou em risco de extinção, classificar em grupos ecológicos e avaliar a estrutura quanto às classes diamétricas e hipsométricas num fragmento de Cerrado de Cariri, Tocantins. Foram mensurados 2.654 indivíduos, distribuídos em 34 famílias, 73 gêneros e 81 espécies. A classe diamétrica predominante dos indivíduos foi 2,5-4,3 cm e hipsométrica de 4,6-8,2 m. Conclui-se que o fragmento é composto por indivíduos predominantemente jovens e o índice sucessional (IS=1,64) caracteriza a população com estágio de sucessão ecológico em fase de transição entre o inicial e o intermediário.
Palavras-chave: Diversidade, Espécies endêmicas, Savana.
Abstract: The objective was to identify the floristic composition, to highlight the rare and/or endangered species, to classify in ecological groups, and to evaluate the structure regarding the diametric and hypsometric classes in a Cerrado fragment of Cariri, Tocantins. We measured 2,654 individuals distributed in 34 families, 73 genres, and 81 species. The predominant diametric class of individuals was 2.5-4.3 cm, and the prevailing hypsometric was 4.6-8.2 m. It is concluded that the fragment is composed of predominantly young individuals and the successional index (SI = 1.64) characterizes the population with an ecological succession stage in the transition phase between the initial and intermediate stages.
Keywords: Diversity, Endemic species, Savannah.
Resumen: El objetivo fue identificar la composición florística, destacar las especies raras y / o en riesgo de extinción, clasificar en grupos ecológicos y evaluar la estructura en cuanto a las clases diamétricas e hipsométricas en un fragmento de Cerrado del Cariri, Tocantins. Se midieron 2654 individuos, distribuidos en 34 familias, 73 géneros y 81 especies. La clase diamétrica predominante de los individuos fue 2,5-4,3 cm e hipsométrica de 4,6-8,2 m. Se concluye que el fragmento está compuesto por individuos predominantemente jóvenes y el índice sucesional (IS = 1,64) caracteriza a la población con etapa de sucesión ecológica en fase de transición entre el inicial y el intermediario.
Palabras clave: Diversidad, Especies endémicas, Sabana.
1 Introdução
O cerrado stricto sensu tem sua vegetação formada por arbustos, arvoretas e um estrato herbáceo dominado por gramíneas, enquanto a vegetação lenhosa é caracterizada por possuir troncos e galhos torcidos, às vezes inclinados. Essa formação é ainda subdividida em cerrado denso, cerrado típico, cerrado ralo e cerrado rupestre, os quais são baseados na densidade dos componentes arbustivo-arbóreo e subarbustivo-herbáceo e nas propriedades do substrato, cuja flora é marcada pela ocorrência do fogo que influencia diretamente a sua composição (RIBEIRO; WALTER, 2008).
A ocorrência do fogo em ambiente de Cerrado é considerada um importante agente evolutivo responsável por alterações florísticas, filogenéticas e funcionais nas comunidades vegetais, altera a composição do solo e modifica as interações entre as espécies. A frequência do fogo é registrada por muitos autores (COUTINHO, 1977; MEIRELLES; HENRIQUES, 1992; MARTINS et al., 2002; RIBEIRO et al., 2012) como forma de reduzir a biomassa seca, favorecer o rebrotamento de algumas espécies, superar a dormência de sementes e também selecionar as espécies mais adaptadas a essas condições de ambiente savânico. No entanto, a ausência do fogo por muitos anos numa determinada área aumenta o risco de ocorrência de incêndios catastróficos. Por outro lado, o uso desse recurso como forma de manejo pode alterar a sucessão das espécies (SILVA et al., 2011), e, nesse sentido, atualmente é necessário que o homem lance mão de estratégias de manejo do fogo a fim de conservar e preservar a biodiversidade.
Para se conservar e preservar os espaços naturais, é necessário entender os processos que ocorrem nos diferentes estágios de sucessão vegetacionais, pois, a partir desses conhecimentos preliminares, estratégias para o manejo e a recuperação de possíveis áreas em risco de degradação ou degradadas podem ser indicadas (SILVA et al., 2012). Dessa forma, analisar a diversidade de espécies, bem como a distribuição diamétrica e hipsométrica de uma população é essencial para compreender o estágio de crescimento e a sucessão ecológica da vegetação (MARANGON et al., 2008; PEREIRA et al., 2010).
Considerando que muitas áreas de Cerrado estão susceptíveis a eventos de fogo natural e também acidental, é possível que a ocorrência do fogo afete a diversidade de espécies e a sucessão natural. Diante do exposto, a presente pesquisa teve por objetivo identificar a composição florística, destacando as espécies em risco, além de classificar em grupos ecológicos e avaliar a sua estrutura com relação às classes diamétrica e hipsométrica em um fragmento de cerrado stricto sensu de Cariri, Tocantins.
2 Material e Métodos
A área de estudo encontra-se localizada no município do Cariri do Tocantins (TO) e abrange uma área de um remanescente florestal de Cerrado com aproximadamente 506 ha (Figura 1). O presente trabalho teve sua etapa de campo realizada durante os dias 5, 6, 7 e 8 de fevereiro de 2015.
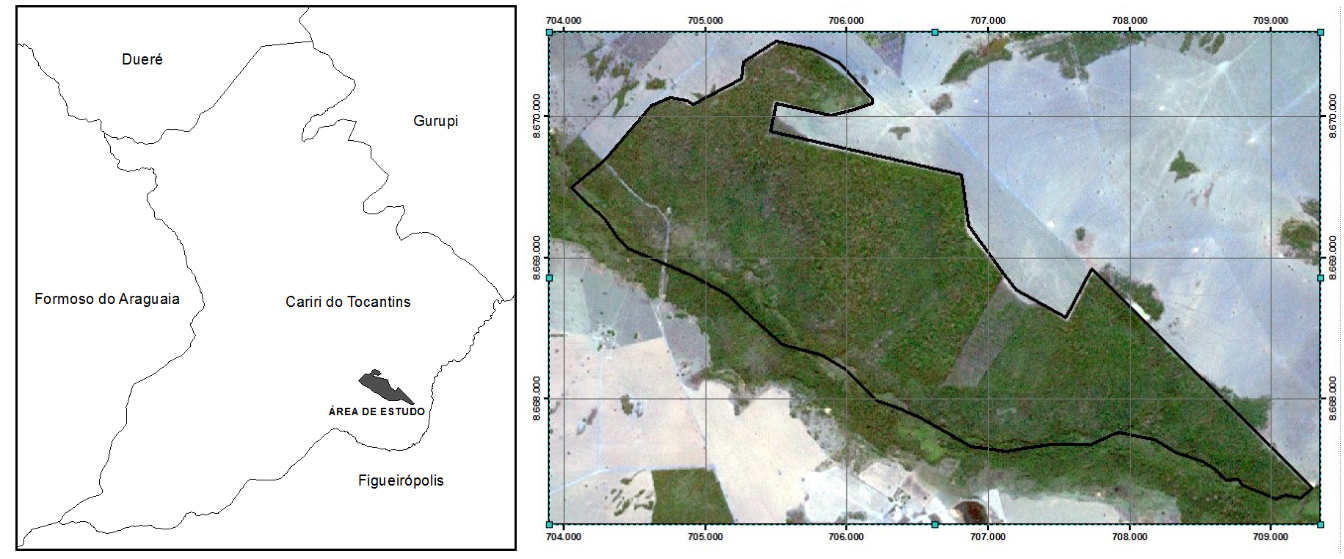
Figura 1.
Localização da área de estudo
De acordo com a Secretaria do Planejamento (SEPLAN, 2012), a área de estudo está inserida no sistema hidrográfico rio Tocantins e na sub-bacia do rio Santo Antônio. De acordo com a classificação climática de Thornthwaite, o clima na região é C2wA’a’’, caracterizado como úmido e subúmido e de moderada deficiência hídrica no inverno, e apresenta evapotranspiração potencial média anual de 1.500 mm.
O solo do município é constituído por Latossolos, Plintossolos e Argissolos. A topografia é plana com grandes áreas de pastagens, em que a agropecuária representa 45,3%, com destaque para a criação de bovinos e o cultivo de milho, mandioca e soja (SEPLAN, 2012).
Para a avaliação da vegetação foi amostrada uma área de 2,75 ha de cerrado stricto sensu do tipo denso, sendo subdividida em 55 parcelas de 500 m² (10 x 50 m) tomando como referência Felfili et al. (2005), nas quais os indivíduos foram identificados, medidos e classificados em grupos ecológicos, destacando também as espécies vegetais raras e aquelas em possíveis riscos de extinção, de acordo com o livro vermelho da flora do Brasil (MARTINELLI et al., 2014), que aborda as plantas raras do Cerrado.
2.1 Variáveis analisadas, identificação e grupos ecológicos
O diâmetro à altura do Peito (DAP) dos indivíduos foi obtido por meio da medição da Circunferência à Altura do Peito (CAP) desses mesmos indivíduos a 1,30 m do nível do solo, sendo o DAP facilmente obtido utilizando a relação entre DAP e CAP, logo:
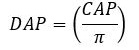 [Eq. 1]
[Eq. 1]Para os indivíduos que não foram identificados em campo, realizou-se a coleta de material botânico, o qual foi utilizado para sua identificação no herbário de Porto Nacional - TO. Para a classificação das famílias botânicas seguiu a classificação Angiosperm Phylogeny Group (APG III, 2009).
Com relação aos grupos ecológicos, as espécies foram separadas em três grupos seguindo a classificação de Gandolfi et al. (1995): a) pioneiras (P) - dependentes de luz que não ocorrem no sub-bosque, desenvolvendo-se em clareiras ou nas bordas da floresta; b) secundárias iniciais (SI) - ocorrem em condições de sombreamento médio ou luminosidade pouco intensa, ocorrendo em clareiras pequenas, bordas de clareiras grandes e bordas de floresta; e c) secundárias tardias (ST) - desenvolvem-se no sub-bosque em condições de sombra leve ou densa e crescem até alcançar o dossel ou a condição de emergente. Aquelas espécies que não puderam ser classificadas foram agrupadas na categoria não-classificada (NC).
Seguindo a metodologia de Petrere Junior et al. (2004), foram adotados três grupos sucessionais para calcular o índice sucessional, por isso as espécies na categoria não-classificada não foram contempladas para esse cálculo. O cálculo do índice sucessional (SI) é dado pela fórmula a seguir:
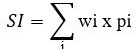
onde:
wi é o número de adaptação clímax já definido (wi =1, 2 e 3);
pi é a porcentagem da espécie j dada pela razão entre o número de indivíduos de uma determinada espécie da população em relação ao total de indivíduos amostrados (pi = ni/ N, onde ni é a abundância de espécies i; e N = número total de indivíduos e s é o número total de espécies no levantamento), sendo assim os valores do SI variam entre 1 e 3, sendo 1 ≤ S I ≤ 3.
3 Resultados e discussão
Foram amostrados 2.654 indivíduos, distribuídos em 34 famílias, 73 gêneros e 81 espécies, destas apenas duas foram identificadas até o táxon gênero (Siphoneugena sp.e Vochysia sp.), sendo também classificadas quanto ao grupo ecológico (Tabela 1). Quanto à representatividade em número de indivíduos, em ordem decrescente, foram Fabaceae (468), Vochysiaceae (464), Rubiaceae (330), Burseraceae (206), Malvaceae (261) e Lytraceae (137). Destacando-se com maior riqueza específica as famílias Fabaceae (18), Malvaceae (6), e Vochysiaceae, Apocynaceae, Euphorbiaceae e Myrtaceae, representadas por quatro espécies cada, além de 20 famílias que foram representadas por apenas uma espécie, sendo por isso consideradas raras nesse fragmento florestal.
| Família | Nome científico | Nome popular | NI | GE |
| Anacardiaceae | Astronium fraxinifolium Schott | Gonçalo-alves | 1 | P |
| Spondias mombin L. | *Cajá | 6 | SI | |
| Annonaceae | Duguetia lanceolata A.St.-Hil. | Ata | 71 | ST |
| Xylopia aromatica (Lam.) Mart. | *Pimenta-de-macaco | 12 | P | |
| Apocynaceae | Aspidosperma cuspa (Kunth) S.F. Blake ex Pittier | Pereira | 6 | SI |
| Aspidosperma macrocarpon Mart. | Guatambu | 1 | SI | |
| Hancornia speciosa Gomes | Mangaba | 1 | ST | |
| Himatanthus obovatus (Müll.Arg.) Woodson | *Pau-de-leite | 53 | ST | |
| Araliaceae | Didymopanax morototoni (Aubl.) Decne. & Planch. | Mandiocão | 3 | SI |
| Arecaceae | Syagrus romanzoffiana (Cham.) Glassman | Baba-de-boi | 8 | SI |
| Bignoneaceae | Paratecoma peroba (Record.) Kuhlm. | Ipê | 21 | SI |
| Tabebuia aurea (Silva Manso) Benth. & Hook. f. ex S. Moore | Caraíba | 15 | ST | |
| Tabebuia ochracea (Cham.) Standl. | *Ipê-amarelo | 2 | SI | |
| Boraginaceae | Cordia trichotoma (Vell.) Arrab. Ex stend. | Freijó | 11 | SI |
| Burseraceae | Tetragastris altissima (Aubl.) Swart | Amescla aroeira | 206 | SI |
| Cannabaceae | Trema micranta (L.) Blume | Candiúva | 1 | P |
| Chrysobalanaceae | Couepia uiti (Mart. & Zucc.) Benth. ex Hook. f. | Pateiro | 3 | P |
| Combretaceae | Buchenavia tomentosa Eichler | *Mirindiba | 11 | SI |
| Terminalia catappa L. | Sete-copas | 1 | ST | |
| Dilleniaceae | Curatella americana L. | *Lixeira | 6 | SI |
| Ebenaceae | Diospyros coccolobifolia Mart. ex Miq. | Olho-de-boi | 16 | SI |
| Euphorbiaceae | Croton urucurana Baill. | Sangra-d’água | 1 | P |
| Sapium argutum (Müll. Arg.) Huber | Burra-leiteira | 10 | NC | |
| Sapium haematospermum Müll.Arg. | Saran | 19 | P | |
| Sebastiania brasiliensis Spreng. | Leiteira | 1 | SI | |
| Fabaceae | Acacia polyphylla DC. | Monjoleiro | 14 | P |
| Amburana cearensis (Allemao) A.C.Smith | Mamoninha | 9 | P | |
| Anadenanthera falcata (Benth.) Speg | *Angico | 3 | SI | |
| Andira cuyabensis Benth. | Angelim | 1 | ST | |
| Apuleia leiocarpa (Vogel) J.F. Macbr. | Amarelão | 15 | SI | |
| Bauhinia mollis (Bong.) D.Dietr. | *Miroró | 35 | P | |
| Caesalpinia echinata Lam. | Pau-de-tinta | 1 | P | |
| Copaifera langsdorffii Desf. | *Pau-de-óleo | 27 | ST | |
| Enterolobium contortisiliquum (Vell.) Morong | *Tamboril | 3 | P | |
| Hymenaea courbaril L. | *Farinheira | 1 | ST | |
| Hymenaea stigonocarpa Mart. ex Hayne | Jatobá | 39 | ST | |
| Inga cylindrica (Vell.) Mart. | Ingá | 186 | P | |
| Machaerium opacum Vogel | *Jacarandá | 1 | P | |
| Mimosa lacticifera Rizzni & Mattos Filho | *Pau-de-espinho | 1 | P | |
| Plathymenia reticulata Benth. | *Amarelinho | 3 | P | |
| Samanea tubulosa (Benth.) Barneby & J.W. Grimes | Bordão-de-velho | 7 | P | |
| Sclerolobium aureum (Tul.) Baill. | *Carvoeiro | 52 | SI | |
| Sclerolobium paniculatum Vogel | *Cachamorra | 70 | P | |
| Icacinaceae | Emmotum nitens (Benth.) Miers | Sobre | 3 | SI |
| Lamiaceae | Vitex polygama Cham | *Tarumã | 4 | SI |
| Lauraceae | Ocotea corymbosa (Meisn.) Mez | Louro | 15 | ST |
| Ocotea megapotamica (Spreng.) Mez | Canela-de-urubu | 16 | SI | |
| Lecythidaceae | Cariniana rubra Gardner ex Miers | *Cachimbeiro | 39 | P |
| Lytraceae | Physocalymma scaberrium Pohl | Cega-machado | 137 | P |
| Malpighiaceae | Byrsonima verbascifolia (L.) L.C.Rich. ex A.Juss | *Murici | 1 | NC |
| Malvaceae | Apeiba tibourbou Aubl | Jangada | 25 | SI |
| Ceiba glaziovii (Kuntze) K.Schum. | Barrigudeira | 1 | ST | |
| Eriotheca candolleana (K.hum.) A. Robyns | Embiruçu | 1 | SI | |
| Eriotheca gracilipes (K.Schum.) A. Robyns | Algodãozinho | 64 | SI | |
| Guazuma ulmifolia Lam. | *Mutamba | 169 | SI | |
| Luehea paniculata Mart. | *Açoita-cavalo | 1 | SI | |
| Meliaceae | Cedrella fissilis Vell. | Cedro | 19 | ST |
| Guarea guidonia (L.) Sleumer | Marinheiro | 44 | SI | |
| Moraceae | Ficus insipida Willd. | Figueira | 2 | ST |
| Maclura tinctoria (L.) D.Don ex Steud. | *Moreira | 17 | P | |
| Myrtaceae | Myrcia amazônica DC | *Goiabinha | 8 | SI |
| Psidium guajava L. | Goiabeira | 9 | SI | |
| Siphoneugena sp. | *Crioli | 6 | NC | |
| Syzygium jambos (L.) Alston | Jambo-da-mata | 1 | SI | |
| Opiliaceae | Agonandra brasiliensis Miers ex Benth. & Hook. f. | *Marfim | 2 | ST |
| Poaceae | Bambusa textilis var. gracilis | Bambuzinho | 77 | NC |
| Polygonaceae | Triplari americana L. | Pau-da-formiga | 66 | P |
| Rubiaceae | Alibertia sessillis (Vell.) Schumann | *Marmelada | 52 | SI |
| Guettarda viburnoides Cham. et Schltr | Veludo | 1 | ST | |
| Rudgea jasminoides (Cham.) Müll.Arg. | *Cafezinho | 277 | SI | |
| Rutaceae | Hortia arborea Engl. | Casca-d’anta | 1 | ST |
| Zanthoxylum rhoifolium Lam. | Mama-de-porca | 56 | SI | |
| Sapotaceae | Pouteria ramiflora (Mart.) Radlk | Grão-de-galo | 1 | ST |
| Pouteria torta (Mart.) Radlk. | *Guapeva | 3 | SI | |
| Urticaceae | Cecropia pachystachia Trécul | Embaúba | 48 | P |
| Pourouma cecropiifolia Mart. | Uvinha | 18 | P | |
| Velloziaceae | Vellozia squamata Pohl | *Canela-de-ema | 52 | NC |
| Vochysiaceae | Callisthene fasciculata Mart. | Capitão | 4 | ST |
| Qualea multiflora Mart. | *Cinzeiro | 317 | P | |
| Qualea parviflora Mart. | *Pau-terra | 140 | P | |
| Vochysia sp. | Cajirana | 3 | NC | |
| Total=34 | 81 | 2654 |
Segundo Haridasan (2005), a abundância de algumas espécies em comunidade de cerrado stricto sensu se deve à vantagem competitiva por serem menos exigentes em nutrientes e por apresentarem menos concentração de nutrientes nas folhas, como as espécies do gênero Qualea. Outro aspecto que contribui para a menor exigência de nutrientes no solo por algumas espécies se deve à capacidade de fixação de nitrogênio por parte das espécies da família Leguminosae, atualmente classificada como Fabaceae, e também à acumulação de alumínio por aquelas pertencentes às famílias Vochysiaceae, Rubiaceae e Melastomataceae, que possuem um mecanismo de adaptação para superar a elevada quantidade desse elemento químico no solo.
As espécies mais representativas desse fragmento de Cerrado são Qualeamultiflora Mart. (317), seguida de Rudgeajasminoides (Cham.) Müll.Arg. (277), Tretragastrisaltissima (Aubl.) Swart Willd. (206), Inga cylindrica (Vell.) Mart. (186), Guazumaulmifolia Lam. (169), Qualea parviflora (Mart.) Warm. (140) e Physocalymmascaberrium Pohl (137) (Tabela 1). Essa tendência de concentração da riqueza em poucas famílias é relatada para a flora arbórea de cerrado stricto sensu por diversos autores (NERI et al., 2007; CARVALHO et al., 2008; MOURA et al., 2010; LOPES et al., 2011), bem como a grande riqueza de espécies concentrada na família Fabaceae e a alta representatividade de indivíduos em Vochysiaceae, a qual foi bem representada pelos três gêneros Callisthene, Qualea e Vochysia. De acordo com Carvalho et al. (2008), a riqueza de espécies lenhosas do cerrado stricto sensu raramente ultrapassa a cota de 100 espécies por hectare. Sendo assim pode-se inferir que esse fragmento estudado apresenta alta riqueza específica.
As espécies deste levantamento, tanto as endêmicas do Cerrado quanto as raras, não apresentam riscos de extinção, tomando como base o livro vermelho da flora do Brasil, que aborda as plantas raras do Cerrado e o Ministério do Meio Ambiente que reconhece as espécies da flora brasileira ameaçadas, exceto Caesalpiniaechinata Lam (MARTINELLI et al., 2014).
Quanto ao grupo ecológico, as espécies foram agrupadas da seguinte forma: 25 (30,86%) pioneiras, 32 (39,51%) secundária inicial, 18 (22,22%) secundária tardia e 6 (7,41%) em não classificadas e, quando considera-se o número de indivíduos, 1.149 (43,29%) são pioneiras, 1.101 (41,48%) secundária inicial, 255 (9,61%) secundária tardia e 149 (5,61%) em não classificadas (Tabela 2). Pelos resultados, nota-se que a distribuição do número de espécies, bem como o número de indivíduos se concentram nas categorias pioneira e secundária inicial, o que reflete a característica da população de transição do estágio pioneiro para o secundário inicial de sucessão ecológica. Tal fato é também confirmado por meio do índice sucessional de 1,64 em que a população apresentou índice compreendido entre 1 e 2.
| Grupo sucessional | Indivíduos | Espécies | % indivíduos | % Espécies |
| Pioneira | 1149 | 25 | 43,29 | 30,86 |
| Secundária inicial | 1101 | 32 | 41,48 | 39,51 |
| Secundária tardia | 255 | 18 | 9,61 | 22,22 |
| Não classificada | 149 | 6 | 5,61 | 7,41 |
| Total | 2654 | 81 | 100 | 100 |
Comparativamente a este estudo, Carvalho e Marques-Alves (2008) também analisaram o índice sucessional (IS) em vegetação de cerrado stricto sensu, na qual encontraram um valor de IS=2,3, indicando que a comunidade apresenta estágio de sucessão intermediário já que o valor oscila entre 1 e 3. Tomando como base o referido autor, sugere-se que a população vegetal de Cariri apresenta um estágio de transição do inicial para o intermediário, pois o IS está próximo de 2. Segundo Petrere Junior et al. (2004), a utilização desse índice é importante como medida direta da proporção das espécies em grupos funcionais e ainda possibilita fornecer uma medida mais realista e operacional para avaliar as mudanças na comunidade durante a sucessão.
O DAP variou de 2,5 a 14,2 cm, com uma média de 4,46 cm para os indivíduos avaliados, sendo que o número de indivíduos reduz à medida que aumenta o número de classes. Apresentou-se, assim, a distribuição no formato de J-invertido com 1.494 indivíduos (56,4 %) agrupados na menor classe diamétrica (2,5 a 4,3 cm) (Figura 2A), comprovando que essa população apresenta estágio jovem pois a maioria dos indivíduos faz parte das menores classes. O padrão de distribuição dos indivíduos em J-invertido ocorre em várias formações de cerrado indicando também o recrutamento dos indivíduos nas classes seguintes para a regeneração da comunidade (ABREU et al., 2012; CASELLA; SILVA JÚNIOR, 2013).
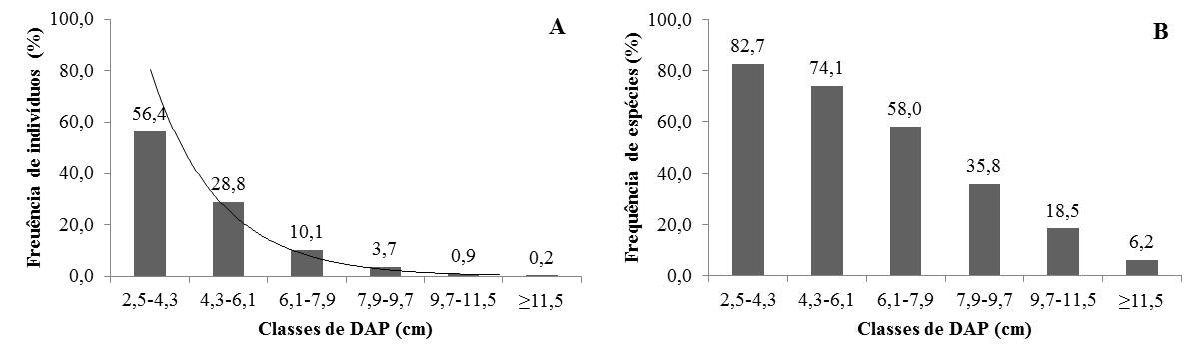
Figura 2.
Frequência de indivíduos (A) e espécies (B) por classes de diâmetro
O número de espécies arbustivo-arbóreas encontradas também tende a reduzir nas classes seguintes de 67 para 5 (82,7 para 6,2%) (Figura 2B), o que indica que muitas espécies têm poucos representantes, o que é confirmado na Tabela 1, já que 20 espécies têm apenas um exemplar, e mais de 20 são representadas por menos de nove indivíduos cada uma. O fato de que 34 espécies (41,97%) amostradas surgem nas últimas classes diamétricas de 7,9 a 11,5 cm sugere que a população seja jovem, já que a maiorias das espécies e indivíduos se encontram em classes menores.
Analisando ainda a distribuição diamétrica por espécies, pode-se observar que apenas 15 apresentaram diâmetro superior a 9,7 cm, representadas por somente 25 indivíduos. Entre as espécies apresentadas, apenas cinco (Hymenaeastigonocarpa Mart. ex Hayne, Tetragastrisaltissima (Aubl.) Swart, Guarea guidonia (L.) Sleumer, Sclerolobium paniculatum Vogel e Inga cylindrica (Vell.) Mart.) mostram tendência de distribuição em forma de J-invertido. Isso sugere que os indivíduos estão se estabelecendo em pequenas proporções (Tabela 3). Entre as espécies avaliadas, Hymenaeastigonocarpa Mart. ex Hayne apresentou o maior diâmetro, com 6,93 cm de média por indivíduos.
| Classes diamétricas (cm) | |||||||
| Espécies | 2,5-4,3 | 4,3-6,1 | 6,1-7,9 | 7,9-9,7 | 9,7-11,5 | ≥11,5 | Total |
| Apuleia leiocarpa (Vogel) J.F. Macbr. | 1 | 5 | 4 | 2 | 2 | 1 | 15 |
| Ceiba glaziovii (Kuntze) K.Schum. | 1 | 1 | |||||
| Copaifera langsdorffii Desf. | 4 | 2 | 11 | 8 | 2 | 27 | |
| Guarea guidonia (L.) Sleumer | 18 | 17 | 5 | 3 | 1 | 44 | |
| Hymenaea courbaril L. | 1 | 1 | |||||
| Hymenaea stigonocarpa Mart. ex Hayne | 3 | 12 | 12 | 8 | 2 | 2 | 39 |
| Inga cylindrica (Vell.) Mart. | 133 | 39 | 9 | 3 | 1 | 1 | 186 |
| Maclura tinctoria (L.) D.Don ex Steud. | 11 | 3 | 1 | 1 | 1 | 17 | |
| Rudgea jasminoides (Cham.) Müll.Arg. | 222 | 44 | 8 | 2 | 1 | 277 | |
| Samanea tubulosa (Benth.) Barneby & J.W. Grimes | 2 | 2 | 2 | 1 | 7 | ||
| Sclerolobium aureum (Tul.) Baill. | 7 | 13 | 15 | 12 | 5 | 52 | |
| Sclerolobium paniculatum Vogel | 9 | 27 | 25 | 6 | 2 | 1 | 70 |
| Tetragastris altissima (Aubl.) Swart | 32 | 85 | 71 | 15 | 3 | 206 | |
| Vellozia squamata Pohl | 37 | 13 | 1 | 1 | 52 | ||
| Zanthoxylum rhoifolium Lam. | 28 | 23 | 4 | 1 | 56 | ||
| Outras espécies | 987 | 463 | 110 | 44 | 0 | 0 | 1604 |
| Total | 1494 | 748 | 278 | 104 | 25 | 5 | 2654 |
Segundo Souza et al. (2012), o padrão de distribuição dos indivíduos no formato de J- invertido é comum em florestas tropicais estáveis com idade e composição de espécies variadas. Neste formato, à medida que o número de classes aumenta, o número de plantas por classe diamétrica reduz. No entanto, quando as espécies são avaliadas individualmente, essa tendência não se mantém, indicando que novos indivíduos estão se estabelecendo na área em menores proporções.
Caso o ambiente sofra alguma perturbação na vegetação que resulte na morte dos indivíduos mais velhos, os demais indivíduos jovens junto com os regenerantes rapidamente recomporão a área afetada. Portanto, esse padrão de distribuição em que a maioria dos indivíduos são agrupados nas menores classes de diâmetro demonstra uma característica de estágio secundário inicial por parte da vegetação avaliada (PEREIRA JUNIOR et al., 2012).
No presente estudo, o maior diâmetro encontrado foi de 14,2 cm e as menores classes de 2,5 a 6,1 cm contemplaram 84,47% da população amostrada (2.242 indivíduos). Por outro lado, no Parque Ecológico dos Pequizeiros, Distrito Federal, também fragmento de cerrado stricto sensu, o diâmetro encontrado por Casella e Silva Júnior (2013) atingiu valores superiores a 35 cm, sendo que os menores centros de classes (5 a 10) corresponderam a 60,86% da vegetação.
Com relação à altura dos indivíduos (Figura 3), a mediana encontrada foi de 6,6 m (mínima= 1,0 e máxima=24,0 m), cuja distribuição também apresenta tendência de formato de J-invertido, em que a maioria dos exemplares representados por 2.021 indivíduos (76,9%) foi agrupada nas menores classes hipsométricas e poucos apresentaram porte maior e/ou estavam em estágio mais avançado de desenvolvimento. Esse padrão de distribuição das alturas também foi verificado por Giácomo et al. (2013) em outra área de cerrado stricto sensu, com as três primeiras classes contemplando a maioria dos indivíduos.
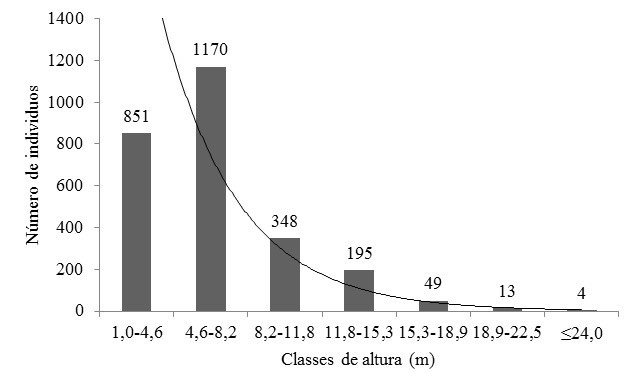
Figura 3.
Frequência de indivíduos por classes de altura hipsométricas
Segundo Marangon et al. (2008), o estudo da estrutura vertical é de suma importância, pois possibilita analisar o estágio de desenvolvimento da floresta baseando-se na distribuição dos indivíduos em diferentes estratos e estágios sucessionais. A existência de baixos valores de diâmetro e altura indicam que a vegetação é composta por indivíduos jovens, o que é confirmado pela distribuição de altura e diâmetro em formato de J-invertido (CARVALHO; MARQUES-ALVES, 2008). Corroborando essa afirmativa, infere-se que a área estudada se enquadra em estágios iniciais de sucessão em virtude de a maioria dos indivíduos estarem alocados nas menores classes diamétricas e hipsométricas.
Diante desses resultados, supõe-se que essa fitofisionomia sofre influência de colonização de espécies de fisionomias próximas e até mesmo de espécies características de outros biomas. Isso se confirma, pois, das 45 espécies que apresentaram as maiores alturas compreendidas entre 17 e 24 m, apenas 18 são peculiares do Cerrado: Anadenanthera falcata (Benth.) Speg, Sclerolobium paniculatum Vogel, Cariniana rubra Gardner ex Miers, Rudgea jasminoides (Cham.) Müll.Arg., Sclerolobium aureum (Tul.) Baill., Spondias mombin L., Qualea multiflora Mart., Hymenaea courbaril L., Cordia trichotoma (Vell.) Arrab. Ex stend., Pouteriatorta (Mart.) Radlk, Machaerium opacum Vogel, Alibertia sessillis (Vell.) Schumann, Buchenaviatomentosa Eichler, Macluratinctoria (L.) D.Don ex Steud., Guazuma ulmifolia Lam., Copaifera langsdorffii Desf. e Xylopia aromatica (Lam.) Mart.
Ainda na classe de altura com variação de 17 a 24, foram encontradas espécies de outros biomas, as quais se apresentam, porém, como acessórias no Cerrado, sendo representadas por: Apuleia leiocarpa (Vogel) J.F. Macbr, Tetragastrisaltissima (Aubl.) Swart, Duguetia lanceolata A.St.-Hil., Sapium argutum (Müll. Arg.) Huber, Callisthene fasciculata Mart., Hortia arborea Engl., Cedrella fissilis Vell., Physocalymma scaberrium Pohl, Cecropia pachystachia Trécul, Ficus insipida Willd., Psidium guajava L., Inga cylindrica (Vell.) Mart., Paratecomaperoba (Record.) Kuhlm., Apeiba tibourbou Aubl, Hymenaea stigonocarpa Mart. ex Hayne, Ocotea corymbosa (Meisn.) Mez, Zanthoxylum rhoifolium Lam., Amburana cearensis (Allemao) A.C.Smith, Didymopanax morototoni (Aubl.), Guarea guidonia (L.) Sleumer, Byrsonima verbascifolia (L.) L.C.Rich. ex A.Juss, Diospyroscoccolobifolia Mart. ex Miq., Couepiauiti (Mart. & Zucc.) Benth., Terminaliacatappa L., Emmotumnitens (Benth.) Miers e Pourouma cecropiifolia Mart.
Segundo Ribeiro e Walter (2008), o cerradão que é um tipo de fitofisionomia de cerrado inserida dentro do cerrado stricto sensu apresenta estrato arbóreo que varia de 7 a 17 m e pode atingir até 20 m de altura, o que sugere que espécies típicas do cerradão também estejam influenciando na estrutura da fitofisionomia estudada. Esse fato é provável tendo em vista que Casella e Silva Júnior (2013) constataram que há similaridade entre as fitofisionomias citadas e florestas adjacentes, assim como por espécies generalistas, corroborando o verificado neste estudo.
Considerando que o cerrado stricto sensu é subdivido em cerrado típico, denso, ralo e rupestre, Pinheiro e Durigan (2012) analisaram a variação estrutural para três condições de cerrado e verificaram que a altura máxima das cinco maiores árvores nas condições de cerrado do tipo típico, denso e cerradão foram 10,0, 12,2 e 17,5 m, respectivamente, enquanto os diâmetros foram 25,6, 33,1 e 34,7 cm.
Ao comparar seis áreas de cerrado distribuídas nos estados de Minas Gerais, Mato Grosso do Sul, Mato Grosso, Tocantins e Piauí e no Distrito Federal, onde se evidenciou a mistura de elementos florísticos de cerrado stricto sensu e formações florestais contendo maior número de espécies savânicas nas áreas de cerradão, Solórzano et al. (2012) constataram a influência de espécies de regiões circunvizinhas e biomas próximos. Os resultados dos referidos autores sugerem a influência das formações vegetais adjacentes e biomas próximos na composição do fragmento de cerrado da região de Cariri, pois foram encontradas espécies generalistas e de porte arbóreo característico de formação florestal.
4 Conclusão
O estudo permite concluir que:
O fragmento de cerrado stricto sensu de Cariri é predominantemente jovem, sendo representado por indivíduos cujas médias de diâmetro e altura são 4,48 cm e 6,6 m, respectivamente.
O posicionamento dos indivíduos arbóreos nas classes iniciais de diâmetro e altura indica que a área se encontra em estágio inicial de sucessão.
O índice sucessional (IS=1,64) caracteriza a população como estágio de transição entre o inicial e o intermediário, sendo representada especialmente pelos grupos ecológicos formados por espécies pioneira e secundária inicial.
A espécie em risco de extinção é a Caesalpinia echinata Lam.
Referências
ABREU, T. A. L. et al. Composição florística e estrutura da vegetação arbustivo-arbórea em Cerrado sentido restrito na serra do Jaraguá, Goiás, Brasil. Heringeriana, v. 6, n. 2, p. 42-53, 2012.
APG III. An update of the angiosperm phylogeny group classification for the orders and families of flowering plants: APG III. Botanical Journal of the Linnean Society, v. 161, n. 2, p. 105-121, 2009.
CARVALHO, A. R.; MARQUES-ALVES, S. Diversidade e índice sucessional de uma vegetação de cerrado sensu stricto na universidade estadual de Goiás-UEG, campus de Anápolis. Revista Árvore, v. 32, n. 1, p. 81-90, 2008.
CARVALHO, F. A. et al. Composição florística, riqueza e diversidade de um cerrado sensu stricto no sudeste do estado de Goiás. Bioscience Journal, v. 24, n. 4, p. 64-72, 2008.
CASELLA, F. M.; SILVA JÚNIOR, M. C. Florística, diversidade e estrutura da vegetação arbórea de cerrado sentido restrito e cerradão adjacentes, parque ecológico dos pequizeiros, Distrito Federal. Heringeriana, v. 7, n. 2, p. 127-142, 2013.
COUTINHO, L. M. Aspectos ecológicos do fogo no cerrado, II: As queimadas e a dispersão de sementes de algumas espécies anemocóricas do estrato herbáceo subarbustivo. Boletim de Botânica da Universidade de São Paulo, v. 5, p. 57-64, 1977.
FELFILI, M. J.; CARVALHO, A. F.; HAIDAR, F. R. Manual para monitoramento de parcelas permanentes nos biomas Cerrado e Pantanal. Brasília: Universidade de Brasília, 2005. 54p.
GANDOLFI, S.; LEITÃO FILHO, H. F.; BEZERRA, C. L. F. Levantamento florístico e caráter sucessional das espécies arbustivo-arbóreas de uma floresta mesófila semidecídua no município de Guarulhos, SE. Revista Brasileira de Biologia, v. 55, n. 4, p. 753-767, 1995.
GIÁCOMO, R. G. et al. Florística e fitossociologia em áreas de campo sujo e Cerrado sensu stricto na estação ecológica de Pirapitinga - MG. Ciência Florestal, v. 23, n. 1, p. 29-43, 2013.
HARIDASAN, M. Competição por nutrientes em espécies arbóreas do Cerrado. In: SCARIOT, A.; SOUSA-SILVA, J. C.; FELFILI, J. M. (Orgs.). Cerrado: ecologia, biodiversidade e conservação. Brasília: Ministério do Meio Ambiente, 2005. p. 168-178.
LOPES, S. F. et al. Análise comparativa da estrutura e composição florística de cerrado no Brasil Central. Interciência, v. 11, n. 1, p. 8-15, 2011.
MARANGON, L. C. et al. Relações florísticas, estrutura diamétrica e hipsométrica de um fragmento de floresta estacional semidecidual em Viçosa (MG). Floresta, v. 38, n. 4, p. 699-709, 2008.
MARTINELLI, G.; MESSINA, T.; SANTOS FILHO, L. Livro vermelho da flora do Brasil: plantas raras do Cerrado. 1. ed. Rio de Janeiro: Instituto de Pesquisas Jardim Botânico do Rio de Janeiro: CNCFlora, 2014. 320p. Disponível em: . Acesso em: 12 ago. 2015.
MARTINS, S. V. et al. Regeneração pós-fogo em um fragmento de floresta estacional semidecidual no município de Viçosa, MG. Ciência Florestal, v. 12, n. 1, p. 12-19, 2002
MEIRELLES, M. L.; HENRIQUES, R. P. Produção primária líquida em área queimada e não queimada de campo sujo de cerrado (Planaltina-DF). Acta Botanica Brasilica, v. 6, n. 2, p. 3-14, 1992.
MOURA, I. O. et al. Diversidade e estrutura comunitária de cerrado sensu stricto em afloramentos rochosos no Parque Estadual dos Pireneus, Goiás. Revista Brasileira de Botânica, v. 33, n. 3, p. 455-467, 2010.
NERI, A. V. et al. Composição florística de uma área de cerrado sensu stricto no município de senador Modestino Gonçalves, Vale do Jequitinhonha (MG) e análise de similaridade florística de algumas áreas de cerrado em Minas Gerais. Revista Árvore, v. 31, n. 6, p. 1109-1119, 2007.
PEREIRA JÚNIOR, L. R.; ANDRADE, A. P.; ARAÚJO, K. D. Composição florística e fitossociológica de um fragmento de caatinga em Monteiro, PB. Holos, Ano 28, v. 6, p. 73-87, 2012.
PEREIRA, I. M. et al. Caracterização ecológica de espécies arbóreas ocorrentes em ambientes de mata ciliar, como subsídio à recomposição de áreas alteradas nas cabeceiras do Rio Grande, Minas Gerais, Brasil. Ciência Florestal, v. 20, n. 2, p. 235-253, 2010.
PETRERE JUNIOR, M.; GIORDANO, L. C.; MARCO JR., P. Empirical diversity index applied to Forest communities in different successional stages. Brazilian Journal of Biology, v. 64, p. 841-851, 2004.
PINHEIRO, E. S.; DURIGAN, G. Diferenças florísticas e estruturais entre fitofisionomias do cerrado em Assis, SP, Brasil. Revista Árvore, v. 36, n. 1, p. 181-193, 2012.
RIBEIRO, J. F.; WALTER, B. M. T. Fitofisionomias do bioma Cerrado. In: SANO, S. M.; ALMEIDA, S. P. & RIBEIRO, J. F. (Ed.). Cerrado: ecologia e flora. Planaltina: EMBRAPA-CPAC, 2008, p. 151-212.
RIBEIRO, M.N. et al. Fogo e dinâmica da comunidade lenhosa em cerrado sentido restrito, Barra do Garças, Mato Grosso. Acta Botanica Brasilica, v. 26, n. 1, p. 203-217, 2012.
SEPLAN. Secretaria do Planejamento. Superintendência de Planejamento e Gestão Central de Políticas Públicas. Diretoria de Zoneamento Ecológico-Econômico (DZE). Base de Dados Geográficos do Tocantins. Palmas: SEPLAN/ DZE, 2012. CD-ROM.
SILVA, D. M. et al. Os Efeitos dos Regimes de Fogo sobre a Vegetação de Cerrado no Parque Nacional das Emas, GO: Considerações para a Conservação da Diversidade. Biodiversidade Brasileira, v.1, n. 2, p. 26-39, 2011.
SILVA, J. C. et al. Sucessão ecológica no cerrado. FLOVET, n. 4, p. 33-47, 2012.
SOLÓRZANO, A. et al. Perfil florístico e estrutural do componente lenhoso em seis áreas de cerradão ao longo do bioma Cerrado. Acta Botânica Brasílica, v. 26, n. 2, p. 328-341, 2012.
SOUZA, P. B.; SOUZA, A. L.; MEIRA NETO, J. A. A. Estrutura diamétrica dos estratos e grupos ecológicos de uma área de floresta estacional semidecidual, em Dionísio, MG. Revista Árvore, v. 36, n. 1, p. 151-160, 2012.
Notas de autor